生活に欠かせない3要素には衣食住がありますが、安全・安心な生活を営むには、これ以外にも医薬品はなくてはならない存在です。医薬品の信頼性を支える3要素は法律名※にもあるとおり品質、有効性及び安全性ですが、普段私たちが薬局やドラッグストア等でよく耳にするのは有効性・安全性です。そこで、ここでは「品質」とりわけ「品質管理」に焦点を当てて説明したいと思います。
※医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和35年法律第145号、旧称:薬事法)
品質管理の重要性
医薬品といえば、本当に効くのか、安全なのかということを気にする人が多いと思います。しかし品質が一定でなければ、安定した有効性や安全性を確保することができません。そのため、品質が定められた範囲(規格)に適合しているかを確認する品質管理は、有効性及び安全性にとってとても重要なものとなります。なお、医薬品の品質規格は各社が独自に設定するだけではなく、有効性及び安全性とともに品目毎に販売前に国で厳しく審査、承認されなければなりません。図1に新医薬品の開発から審査、承認及び販売に至る創薬の過程を示しました。
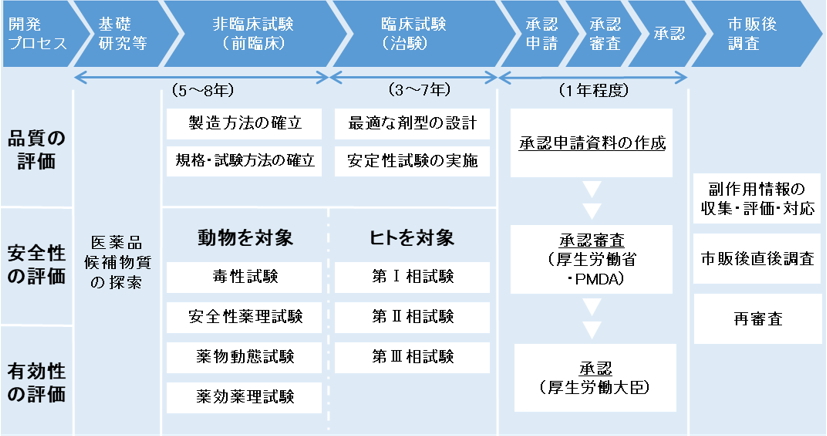
図1 新医薬品の開発から承認審査・調査の体制
(独立行政法人 医薬品医療機器総合機構及び厚生労働省の資料より作成)
品質管理すべき項目について
医薬品の品質を適正に確保するために、必要な規格・基準及び標準的試験方法等を示した公的な規範書として日本薬局方が定められています。その中で、医薬品の品質管理項目として有効成分の含量、確認試験、純度、均一性及び溶出性などが記載されていますが、その代表例を次に示します。
「含量」は、医薬品中の有効成分の量を表し、有効成分の特性により物理的、化学的又は生物学的方法を用いて測定します。許容される管理幅は、日本薬局方収載医薬品では±5%、±10%など厳しく設定されています。例えば、有効成分が5mg配合で許容幅が±5%の医薬品の場合、平均含量の値は5±0.25mgとごくわずかな範囲の中に入っている必要があります。
「純度試験」は、医薬品中の不純物を確認するために行うもので、ほかの試験と共に、医薬品の純度を規定する試験です。不純物の種類及びその量の限度が規定されます。不純物は目的をもって配合される有効成分や添加剤とは異なり、毒性を示す物質もあり、品質管理上、厳しく制限する必要があります。この試験の対象となる不純物とは、あくまでその医薬品を製造する過程又は保存の間に混在が予想されるもので、例えば、有効成分を化学合成する際に発生し、除くことができなかった副生成物などです。残念ながら想定外の混入物については、必ずしも確認できるとは限りませんので、他の試験や各記録のチェックなどで総合的に判断することが重要です。
「溶出試験」はその名のとおり、口から摂取する医薬品を対象に溶出試験器(図2)を用いて試験検査を行い、有効成分の溶出率を確認する試験です。

図2 溶出試験器(左)と錠剤の溶出試験(拡大)(右)
その医薬品が設計されたとおりに、一定量の有効成分が体内の特定の場所で溶け出すかの指標となります。日本においては、製剤の“著しい生物学的非同等を防ぐ”ことを目的とした試験でもあります。後発医薬品(ジェネリック医薬品)では、各条件で標準とした製剤(先発医薬品)との溶出挙動の類似性を確認するなどがガイドラインに示されています。厚生労働省が設置したジェネリック医薬品品質情報検討会では、液性の異なる複数の試験液を用いて先発医薬品と後発医薬品との溶出挙動等の比較確認を行っており、その結果及び関連情報はブルーブックとして検討会のホームページで確認することができます(図3)。
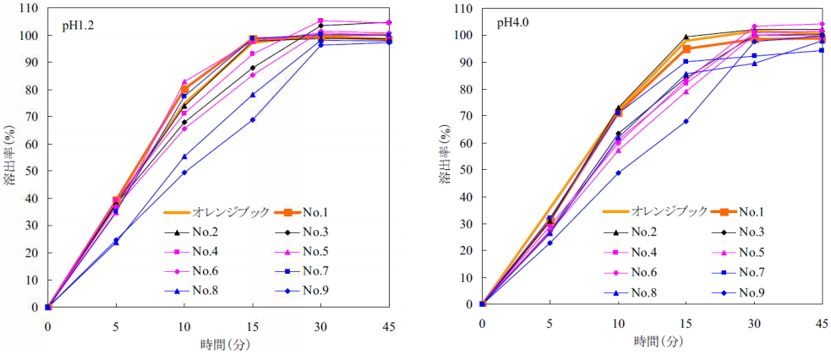
図3 アカルボース錠(糖尿病治療薬)の溶出挙動の比較例
(第11回ジェネリック医薬品品質情報検討会資料11-1より)
また、医薬品は包装の中身(錠剤、注射液など)だけではなく、その包装(シート状のPTP包装、ガラス製のアンプルなど)自体も「製剤包装」として厳しく品質管理されます。包装は医薬品を光、湿度又は微生物などから守り、製造後、患者が服用するまでの一定期間、品質及び有効性などの安定性を担保するためにも重要な資材です。包装適格性が確認された資材等に管理すべき項目を設定します。その項目は、最終的に製剤の安定性の確認により評価します。
何種類かの試験を紹介しましたが、数多くある医薬品に関する試験項目のわずか一部です。このように、各医薬品はそれぞれの特性により多くの品質管理項目が設定され、製造毎に試験検査が実施され、品質が管理されています。
神奈川県衛生研究所における取組
神奈川県には多くの医薬品製造所があり、先発医薬品から後発医薬品、有効成分である原薬など多種にわたる医薬品が製造され、試験検査にて品質を確認後、出荷されています。
神奈川県では、県内の医薬品製造所等に対し、立ち入り調査を行い製造管理及び品質管理の状況を監視しています。また、必要に応じて法律に基づく収去を実施し、当所でその検体の試験検査を実施することで、流通医薬品の品質の確認を行っております。
安心してお使いいただくために
医薬品はその他の製品と異なり、患者からは選択する余地が少ないため、品質、有効性及び安全性が確保された医薬品のみが流通しなければなりません。そのため、原料の製造から製品の流通、市販後の安全性に係る調査に至るまで徹頭徹尾、有資格者による管理の徹底が求められています。また、最終的に有効性及び安全性を確保するためには、患者自身も知識と理解を深め、医薬品を適正に使用する必要があります。
また、代替品がない医薬品も多いため、管理の不備により製品回収となり、医療現場から無くなるといった状況は避けなければなりません。近年、品質管理の不備から起こる回収事例も散見されることから、県内事業者の皆様には改めて製造管理・品質管理の徹底をお願いするとともに、当所でも更なる公衆衛生の向上と確保のために試験検査や調査研究を全力で取り組んでいきたいと思います。
【参考リンク及び文献】
- 独立行政法人 医薬品医療機器総合機構(PMDA)ホームページ

- 第十七改正日本薬局方(平成28年3月7日厚生労働省告示第64号)
- 後発医薬品の生物学的同等性試験ガイドライン(国立医薬品食品衛生研究所)

- ジェネリック医薬品品質情報検討会

(理化学部 岩橋 孝祐)
|
|||||||||||

